海南这些医疗器械不合格,半数来自这家公司
3月5日上午,记者从海南省药品监督管理局了解到,该局组织对桡动脉压迫止血带、一次性使用无菌注射器带针、金属骨针、定制式固定义齿、低密度脂蛋白胆固醇测定试剂盒(LDL-C)、软性接触镜(隐形眼镜、美瞳等),腹膜透析管路、医用外科口罩等38个品种195批产品进行质量监督抽检,其中4个品种6批次不合格。一次性使用透析护理包、腹膜透析管路、一次性使用人体静脉血样采集容器、天然胶乳橡胶避孕套这些医疗器械产品不合格。
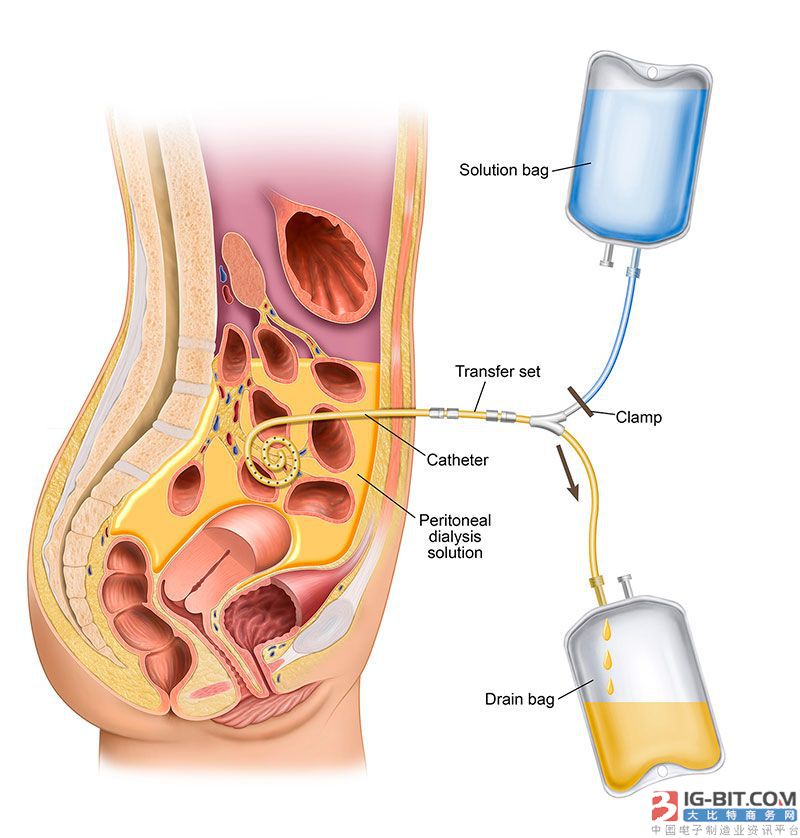
被抽验项目不符合标准规定的医疗器械产品,涉及本省1家医疗器械生产企业的1个品种3批次;外省3家医疗器械生产企业的3个品种3批次。
记者注意到,6批次医疗器械产品不合格,其中3批次不合格产品是由海南朗腾医疗设备有限公司生产。不合格医疗器械产品为一次性使用透析护理包、腹膜透析管路、一次性使用人体静脉血样采集容器、天然胶乳橡胶避孕套,由海南朗腾医疗设备有限公司、吉林省迈达医疗器械股份有限公司、珠海康德莱医疗器械有限公司、东洋构浦乳胶(锦州)有限公司这4家企业生产。
抽检不符合标准规定产品具体情况为:
一、一次性使用透析护理包1家企业3批次产品。海南朗腾医疗设备有限公司生产的3批次一次性使用透析护理包酒精棉球环氧乙烷残留量不符合标准规定。规格型号均为HL-02,生产日期分别为2019年08月31日、2019年08月29日、2019年08月30日,批号分别为20190817、20190815、20190816。
二、腹膜透析管路1家企业1批次产品。吉林省迈达医疗器械股份有限公司生产(规格型号:FMG-2000V1,生产日期/批号:20190423/20190423)的腹膜透析管路接头环氧乙烷残留量不符合标准规定。
三、一次性使用人体静脉血样采集容器1家企业1批次产品。珠海康德莱医疗器械有限公司生产(规格型号:2ml,生产日期/批号:20190320/批190320)的一次性使用人体静脉血样采集容器液体添加剂体积最大容许公差不符合标准规定。
四、天然胶乳橡胶避孕套1家企业1批次产品。东洋构浦乳胶(锦州)有限公司生产(规格型号:长度≥160mm宽度:52±2mm,生产日期/批号:201710/71015)的天然胶乳橡胶避孕套针孔不符合标准规定。
海南省药品监督管理局表示,对上述监督抽检中发现的不符合标准规定产品及有关生产企业、经营企业和使用单位,已严格依照《医疗器械监督管理条例》《医疗器械召回管理办法》等法规规章予以查处并向社会公布,同时督促相关企业查明原因、限期整改,对已上市的不合格产品采取相应的召回纠正措施确保产品的质量安全有效。


 Advisory Hotline:400-123-4567
Advisory Hotline:400-123-4567